Soojusõpetus on füüsika üks komplekssemaid valdkondi. Selle alla mahuvad molekulaarfüüsika, termodünaamika, molekulaarkineetiline teooria ja aine ehitus.
Plokkskeemina võib seda ette kujutada järgmiselt:
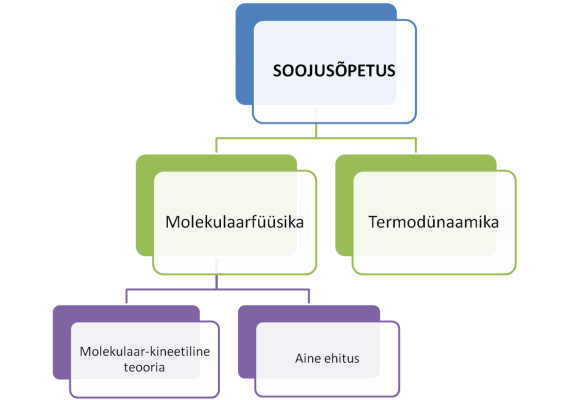
Plokkskeemina võib seda ette kujutada järgmiselt:
Joonis 1. Soojusõpetuse valdkonnad
Molekulaarfüüsikat tutvustavad eelmises õpiobjektis "Sissejuhatus füüsikasse" esitatud mõned näited. Molekulaarfüüsika käsitleb gaaside, vedelike ja tahkiste füüsikalisi omadusi sõltuvalt aine molekulaarsest ehitusest. Terminite "tahke keha" ja "tahkis" kasutamisel esineb tihti arusaamatusi. Tahkis on kristalliline aine ja tal on kindel sulamistemperatuur (näiteks jää). Tahkis on ka tahke aine. Aga osa tahkeid aineid, niinimetatud amorfsed ained (näiteks klaas) on sisuliselt vedelikud erakordselt suure viskoossusega. Nendel puudub kindel sulamistemperatuur.
Molekulaarfüüsika alla kuuluvad 1) molekulaar-kineetiline teooria ehk molekulide liikumist kirjeldav teooria ja 2) aine ehitus, mis, nagu nimigi ütleb, uurib aine sisemist struktuuri ja struktuurseid muutusi aines. Termodünaamika uurib soojusnähtusi ja nende seost aine füüsikalis-keemiliste omadustega. Nagu näha, on kõik need soojusõpetuse alaosad omavahel väga seotud. Edaspidises selgub kõik täpsemalt.
Temperatuur ja soojus
Mõisteid "temperatuur" ja "soojus" kiputakse ära segama. Keha temperatuuri määrab tema molekulide keskmine kineetiline energia. Paneme tähele, et "määrab ära", aga ei ole molekulide keskmine kineetiline energia. Temperatuur ei ole energia, vaid temperatuur on keha soojusliku oleku aste. Soojus aga on energia. Füüsikas on täpsem öelda "soojushulk Q". Soojusenergia või soojushulga ülekandumine muudab kehade temperatuure. Sõna "soojus" on pärit kõnekeelest ja seda sõna kasutatakse ka füüsikas, aga soojus ei ole füüsikaline suurus. Füüsikas väljendatakse keha soojendamist keha siseenergia suurendamisena. Soojushulk Q on siseenergia, mille keha saab või ära annab.
Soojushulka kui füüsikalist suurust mõõdetakse džaulides (1J) või kalorites (cal). 1cal = 4,1868 J. Igapäevases elus on ühik 1 J peaaegu tundmatu ning energia mõõtühikuna kasutatakse kilokalorit (kcal), eriti toidu energeetilise väärtuse arvutamisel. 1kcal = 1000 cal = 4,1868 kJ.
Mida tähendab absoluutne temperatuur ja selle skaala ?
Oleme tuttavad temperatuuri mõõtmise Celsiuse skaalaga. Selle skaala aluseks on vesi oma külmumispunktiga 0 C (olen unustanud mõlemad 4-numbrilised koodid kraadi nullikese kirjutamiseks, kusjuures vanasti kirjutati see nullike arvu juurde, aga nüüd juba mõnda aega C juurde ja arvu järel lüüakse lünk) ja keemispunktiga 100 C. Vahel küsitakse, millest on tulenenud nende punktide juures olevad arvud nii ilusad ja ümmargused 0 ja 100. See on lihtsalt sellest, et nendele vee põhipunktidele pani rootsi teadlane Anders Celsius "nimedeks" 0 ja 100 ning jagas nende vahemiku 100-ks osaks ehk kraadiks.
Mis aga on absoluutne temperatuur ja selle skaala ? Kunagi hakati keha temperatuuri seostama keha molekulide soojusliikumisega. Mida kiiremini keha molekulid liiguvad, seda kõrgem on keha temperatuur. Minnes molekulide kiiruse vähenemisega 0-ni ehk molekulide paigale tardumiseni, nimetati sellele olukorrale vastavat temperatuuri absoluutseks 0-temperatuuriks ja vastavat temperatuuriskaalat absoluutse temperatuuri skaalaks. Kuna kõnealuse ettepaneku tegi inglise füüsik lord Kelvin, kodanikunimega William Thomson (1824-1907) 1848.aastal ja nimetas selle temperatuuriskaala absoluutse temperatuuri skaalaks, siis nimetatakse seda skaalat Kelvini skaalaks. Selle skaala üks kraad on võrdne Celsiuse skaala ühe kraadiga. Kraadi märki ehk nullikest Kelvini kraadi K juures ei kasutata. Absoluutset 0-i tähistab sümbol O K (nagu inglise keeles okey). Celsiuse 0 C on ligikaudu 273 K. Celsiuse skaala temperatuuri tähis väike täht t saab Kelvini skaalas tähiseks suur täht T. Niisiis T=273+t. Absoluutne 0 on Celsiuse skaalas -273 C, see tähendab O K= -273 C. Jätame meelde, et Celsiuse skaala kraadi nullikese kirjutame C juurde ning kraadide arvu järel lööme lünga.
Molekulaarfüüsikat tutvustavad eelmises õpiobjektis "Sissejuhatus füüsikasse" esitatud mõned näited. Molekulaarfüüsika käsitleb gaaside, vedelike ja tahkiste füüsikalisi omadusi sõltuvalt aine molekulaarsest ehitusest. Terminite "tahke keha" ja "tahkis" kasutamisel esineb tihti arusaamatusi. Tahkis on kristalliline aine ja tal on kindel sulamistemperatuur (näiteks jää). Tahkis on ka tahke aine. Aga osa tahkeid aineid, niinimetatud amorfsed ained (näiteks klaas) on sisuliselt vedelikud erakordselt suure viskoossusega. Nendel puudub kindel sulamistemperatuur.
Molekulaarfüüsika alla kuuluvad 1) molekulaar-kineetiline teooria ehk molekulide liikumist kirjeldav teooria ja 2) aine ehitus, mis, nagu nimigi ütleb, uurib aine sisemist struktuuri ja struktuurseid muutusi aines. Termodünaamika uurib soojusnähtusi ja nende seost aine füüsikalis-keemiliste omadustega. Nagu näha, on kõik need soojusõpetuse alaosad omavahel väga seotud. Edaspidises selgub kõik täpsemalt.
Temperatuur ja soojus
Mõisteid "temperatuur" ja "soojus" kiputakse ära segama. Keha temperatuuri määrab tema molekulide keskmine kineetiline energia. Paneme tähele, et "määrab ära", aga ei ole molekulide keskmine kineetiline energia. Temperatuur ei ole energia, vaid temperatuur on keha soojusliku oleku aste. Soojus aga on energia. Füüsikas on täpsem öelda "soojushulk Q". Soojusenergia või soojushulga ülekandumine muudab kehade temperatuure. Sõna "soojus" on pärit kõnekeelest ja seda sõna kasutatakse ka füüsikas, aga soojus ei ole füüsikaline suurus. Füüsikas väljendatakse keha soojendamist keha siseenergia suurendamisena. Soojushulk Q on siseenergia, mille keha saab või ära annab.
Soojushulka kui füüsikalist suurust mõõdetakse džaulides (1J) või kalorites (cal). 1cal = 4,1868 J. Igapäevases elus on ühik 1 J peaaegu tundmatu ning energia mõõtühikuna kasutatakse kilokalorit (kcal), eriti toidu energeetilise väärtuse arvutamisel. 1kcal = 1000 cal = 4,1868 kJ.
Mida tähendab absoluutne temperatuur ja selle skaala ?
Oleme tuttavad temperatuuri mõõtmise Celsiuse skaalaga. Selle skaala aluseks on vesi oma külmumispunktiga 0 C (olen unustanud mõlemad 4-numbrilised koodid kraadi nullikese kirjutamiseks, kusjuures vanasti kirjutati see nullike arvu juurde, aga nüüd juba mõnda aega C juurde ja arvu järel lüüakse lünk) ja keemispunktiga 100 C. Vahel küsitakse, millest on tulenenud nende punktide juures olevad arvud nii ilusad ja ümmargused 0 ja 100. See on lihtsalt sellest, et nendele vee põhipunktidele pani rootsi teadlane Anders Celsius "nimedeks" 0 ja 100 ning jagas nende vahemiku 100-ks osaks ehk kraadiks.
Mis aga on absoluutne temperatuur ja selle skaala ? Kunagi hakati keha temperatuuri seostama keha molekulide soojusliikumisega. Mida kiiremini keha molekulid liiguvad, seda kõrgem on keha temperatuur. Minnes molekulide kiiruse vähenemisega 0-ni ehk molekulide paigale tardumiseni, nimetati sellele olukorrale vastavat temperatuuri absoluutseks 0-temperatuuriks ja vastavat temperatuuriskaalat absoluutse temperatuuri skaalaks. Kuna kõnealuse ettepaneku tegi inglise füüsik lord Kelvin, kodanikunimega William Thomson (1824-1907) 1848.aastal ja nimetas selle temperatuuriskaala absoluutse temperatuuri skaalaks, siis nimetatakse seda skaalat Kelvini skaalaks. Selle skaala üks kraad on võrdne Celsiuse skaala ühe kraadiga. Kraadi märki ehk nullikest Kelvini kraadi K juures ei kasutata. Absoluutset 0-i tähistab sümbol O K (nagu inglise keeles okey). Celsiuse 0 C on ligikaudu 273 K. Celsiuse skaala temperatuuri tähis väike täht t saab Kelvini skaalas tähiseks suur täht T. Niisiis T=273+t. Absoluutne 0 on Celsiuse skaalas -273 C, see tähendab O K= -273 C. Jätame meelde, et Celsiuse skaala kraadi nullikese kirjutame C juurde ning kraadide arvu järel lööme lünga.